معرفی فلز مس
مس، عنصری شیمیایی با نماد Cu و عدد اتمی ۲۹، از دیرباز به عنوان یکی از نخستین فلزاتی که توسط بشر کشف و مورد استفاده قرار گرفته، جایگاه ویژهای در تاریخ تمدن بشری داشته است. شواهد باستانشناسی نشان میدهد که استفاده از مس به بیش از ۱۰,۰۰۰ سال پیش از میلاد مسیح در مناطق مختلف جهان، از جمله شمال عراق کنونی، بازمیگردد.
در ایران نیز، قدمت استفاده از این فلز گرانبها به حدود ۷۰۰۰ سال پیش و به معدن مس سیامکو در لرستان میرسد. تمدنهای باستانی در بینالنهرین، مصر، آسیا و اروپا، از مس برای ساخت ابزارآلات ساده، سلاحها، زیورآلات و حتی سیستمهای لولهکشی ابتدایی بهره میبردند.
مس که در گروه ۱۱ جدول تناوبی عناصر قرار دارد، با نماد شیمیایی Cu و عدد اتمی ۲۹ شناخته میشود. نام این عنصر از واژه لاتین “cuprum” مشتق شده است که خود از نام جزیره قبرس گرفته شده است؛ چرا که در دوران امپراتوری روم، این جزیره به عنوان منبع اصلی استخراج مس شناخته میشد. مس یک فلز انتقالی با ساختار کریستالی نرم و خمیدنی است و از ویژگیهای بارز آن میتوان به چکشخواری و مفتولپذیری بالا و همچنین رسانایی الکتریکی و حرارتی فوقالعاده اشاره کرد.

دسترسی و منابع مس
مس به طور طبیعی در پوسته زمین و در ساختار خاک و سنگها یافت میشود و برای دستیابی به آن، از معادن مس استخراج میگردد. کانسارهای مهم مس معمولاً شامل ترکیبات سولفیدی مانند کالکوپیریت، بورنیت، کوولیت و کالکوزین و همچنین ترکیبات اکسیدی نظیر کوپریت، مالاکیت و آزوریت هستند. بزرگترین معادن مس جهان در کشورهایی مانند شیلی، ایالات متحده آمریکا، اندونزی و پرو قرار دارند و ایران نیز با دارا بودن حدود ۳ درصد از ذخایر مس جهان، از اهمیت قابل توجهی در این زمینه برخوردار است.
علاوه بر کانسارها، مس ممکن است به صورت خالص و بدون ترکیب با سایر مواد معدنی نیز در طبیعت یافت شود که به آن “مس خام” گفته میشود. بررسیها نشان میدهد که حدود نیمی از کل ذخایر مس کره زمین در چهار منطقه اصلی شامل آمریکای جنوبی، آسیای مرکزی جنوبی، هندوچین و آمریکای شمالی متمرکز شده است.
رنگ مس خالص و تازه اکسید نشده، صورتی-نارنجی است، اما به سرعت در معرض هوا واکنش نشان داده و لایهای از اکسید قهوهای مایل به قرمز بر روی آن تشکیل میشود. در میان فلزات خالص، مس پس از نقره، به عنوان دومین رسانای برتر الکتریسیته و حرارت شناخته میشود.
این فلز به آسانی قابلیت خم شدن و تغییر شکل را دارد که به این ویژگیها چکشخواری و شکلپذیری بالا گفته میشود. علاوه بر این، مس در برابر خوردگی ناشی از هوا و آب نیز مقاومت خوبی از خود نشان میدهد. یکی دیگر از ویژگیهای مهم مس، قابلیت بازیافت کامل آن است که آن را به مادهای پایدار و سازگار با محیط زیست تبدیل میکند. همچنین، مس به عنوان یک عنصر ضروری برای سلامت بدن انسان شناخته شده و در عملکرد صحیح بسیاری از آنزیمها نقش حیاتی ایفا میکند.
تاریخچهی مس
حدود ۴۰۰۰ سال قبل از میلاد، کشف آلیاژ برنز، که از ترکیب مس و قلع به دست میآمد، نقطه عطفی در تاریخ متالورژی محسوب میشود و دورهای به نام عصر برنز را رقم زد. در مصر باستان، این فلز نه تنها به دلیل کاربردهای فراوانش، بلکه به عنوان نمادی از جاودانگی و عنصری مرتبط با فرعون، از اهمیت ویژهای برخوردار بود.
با گذر زمان و پیشرفت دانش بشری، کاربردهای مس نیز گسترش یافت؛ به طوری که در قرن پانزدهم میلادی، اختراع صنعت چاپ، تقاضا برای مس را به دلیل سهولت حکاکی بر روی صفحات مسی افزایش داد. جالب توجه است که بیش از ۹۵ درصد از کل مس استخراج شده در طول تاریخ، پس از سال ۱۹۰۰ میلادی به دست آمده است. این امر نشاندهنده نقش روزافزون این فلز در صنایع نوین است.
مشاهده بیشتر: داستان کامل پیدایش و کاشف مس
تاریخچه طولانی استفاده از مس نشاندهنده اهمیت اساسی آن برای تمدن بشری به دلیل ترکیب منحصربهفرد خواصش است. گذار از عصر حجر به عصر برنز به خوبی نقش محوری مس را در پیشرفتهای فناورانه نشان میدهد. توزیع جغرافیایی گسترده منابع مس نیز احتمالاً به کشف و استفاده زودهنگام آن توسط تمدنهای باستانی مختلف در سراسر جهان کمک کرده است. وجود هر دو نوع کانسنگ سولفیدی و اکسیدی، روشهای استخراج متفاوتی را ضروری میسازد که در طول زمان توسعه یافتهاند.
ویژگیهای اساسی مس، به ویژه رسانایی الکتریکی و حرارتی بالا، چکشخواری، مفتولپذیری و مقاومت در برابر خوردگی، به طور مداوم در منابع مختلف مورد تاکید قرار گرفتهاند که اهمیت آنها را در کاربردهای گسترده نشان میدهد. این واقعیت که مس برای عملکردهای بیولوژیکی ضروری است و به طور کامل قابل بازیافت است، اهمیت چندوجهی آن را فراتر از کاربردهای صنعتی افزایش میدهد.
ویژگی های فیزیکی فلز مس
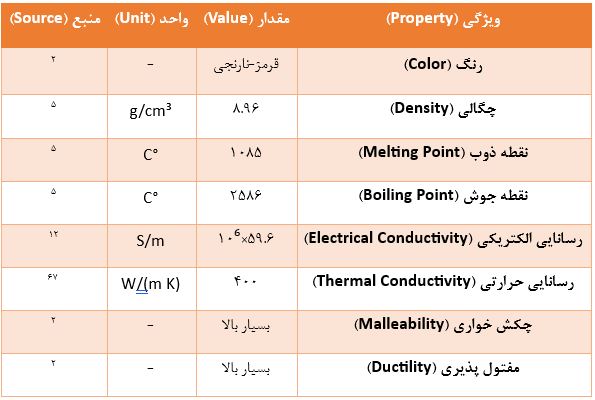
مس دارای مجموعهای از ویژگیهای فیزیکی منحصربهفرد است که آن را برای کاربردهای متنوعی مناسب میسازد.
رنگ
رنگ مس معمولاً قرمز-نارنجی توصیف میشود، اما میتواند به صورت قرمز مایل به قهوهای نیز ظاهر شود. در حالت خالص و قبل از اکسید شدن، مس در واقع دارای رنگ صورتی است. با این حال، به دلیل واکنش سریع با اکسیژن موجود در هوا، معمولاً به رنگ قرمز مایل به قهوهای دیده میشود. با گذشت زمان و در اثر اکسیداسیون، رنگ مس میتواند به سبز یا آبی تغییر کند. این تغییر رنگ ناشی از تشکیل لایهای از کربنات مس یا سایر ترکیبات است.
چگالی
چگالی مس در حدود ۸.۹۶ گرم بر سانتیمتر مکعب در دمای اتاق است. برخی منابع دیگر مقادیر نزدیک به این عدد مانند ۸.۹ گرم بر سانتیمتر مکعب یا ۸.۹۲ گرم بر سانتیمتر مکعب را ذکر کردهاند. چگالی مس در دمای ۲۰ درجه سانتیگراد، ۸.۹۳۵ گرم بر سانتیمتر مکعب گزارش شده است و در حالت مایع و در نقطه ذوب، این مقدار به ۸.۰۲ گرم بر سانتیمتر مکعب کاهش مییابد. چگالی نسبتاً بالای مس باعث میشود که در برابر نیروهای مکانیکی و فشارهای فیزیکی مقاومت خوبی داشته باشد.
نقطه ذوب
نقطه ذوب مس معمولاً در حدود ۱۰۸۵ درجه سانتیگراد ذکر میشود. مقادیر دقیقتری نیز گزارش شده است، از جمله ۱۰۸۴ درجه سانتیگراد و ۱۰۸۴.۶۲ درجه سانتیگراد. برخی منابع بازه ۱۰۸۳.۲ تا ۱۰۸۳.۶ درجه سانتیگراد را برای نقطه ذوب مس ذکر کردهاند. بر اساس مقیاس کلوین، نقطه ذوب مس ۱۳۵۷.۷۷ کلوین (معادل ۱۰۸۴.۶۲ درجه سانتیگراد یا ۱۹۸۴.۳۲ درجه فارنهایت) است. برخی دیگر مقدار ۱,۰۸۳ درجه سانتیگراد (۱,۹۸۱ درجه فارنهایت) را گزارش کردهاند.
نقطه جوش
نقطه جوش مس در حدود ۲۵۸۶ درجه سانتیگراد گزارش شده است. مقادیر دیگری نیز مانند ۲۵۶۲ درجه سانتیگراد و ۲۸۳۵ کلوین (معادل ۲۵۶۲ درجه سانتیگراد یا ۴۶۴۳ درجه فارنهایت) نیز ذکر شده است. بر اساس برخی منابع، نقطه جوش مس ۲۵۶۷ درجه سانتیگراد (۴۶۵۳ درجه فارنهایت) است، در حالی که برخی دیگر مقدار ۲۵۹۵ درجه سانتیگراد را گزارش کردهاند. نقطه جوش مس بر اساس مقیاس کلوین، ۲۸۳۳ کلوین (معادل ۲۵۶۰ درجه سانتیگراد یا ۴۶۴۰ درجه فارنهایت) نیز گزارش شده است.
رسانایی الکتریکی
مس به عنوان یک رسانای الکتریکی بسیار عالی شناخته میشود و پس از نقره، در رتبه دوم در بین فلزات خالص قرار دارد. رسانایی الکتریکی مس در حدود ۵۹.۶×۱۰⁶ زیمنس بر متر است. مس بازپخت شده به عنوان معیار استاندارد بینالمللی برای مقایسه با سایر رساناهای الکتریکی در نظر گرفته میشود و رسانایی آن ۱۰۰% IACS (استاندارد بینالمللی مس بازپخت شده) در دمای ۲۰ درجه سانتیگراد است. مقاومت الکتریکی مس در دمای ۲۰ درجه سانتیگراد، ۱۶.۷۸ نانواهم در متر است.

رسانایی حرارتی
مس علاوه بر رسانایی الکتریکی بالا، رسانای حرارتی بسیار خوبی نیز محسوب میشود و پس از نقره، در رتبه دوم در بین فلزات خالص قرار دارد. رسانایی حرارتی مس تقریباً دو برابر آلومینیوم و ۳۰ برابر فولاد زنگ نزن است. مقدار رسانایی حرارتی مس در حدود ۴۰۰ وات بر متر-کلوین گزارش شده است و مقدار دقیقتری نیز برابر با ۳۸۵ وات بر متر-کلوین ذکر شده است.
چکش خواری و مفتول پذیری
مس فلزی بسیار چکشخوار و مفتولپذیر است، به این معنی که میتوان آن را به راحتی به شکلهای مختلف درآورد و به صورت سیمهای نازک کشید بدون اینکه شکسته شود. این ویژگیها باعث میشود که مس به راحتی کشیده، قالبریزی و شکل داده شود. مس خالص به عنوان یک فلز نرم و چکشخوار با قابلیت شکلپذیری بالا توصیف میشود.
ویژگی های شیمیایی فلز مس
مس علاوه بر ویژگیهای فیزیکی برجسته، دارای خصوصیات شیمیایی قابل توجهی نیز میباشد.
واکنش پذیری
مس به عنوان یک فلز واسطه، واکنشپذیری نسبتاً کمی دارد. این فلز در شرایط معمولی با آب واکنش نمیدهد، اما به آرامی با اکسیژن موجود در هوا واکنش نشان داده و لایهای محافظ از اکسید قهوهای-سیاه بر روی سطح خود تشکیل میدهد که از خوردگی بیشتر جلوگیری میکند. مس همچنین میتواند با برخی ترکیبات گوگرد واکنش داده و سولفیدهای مس را به وجود آورد.
در حالی که مس با اسیدهای غیر اکسید کننده رقیق در غیاب هوا واکنش نشان نمیدهد، به راحتی در اسید نیتریک و اسید سولفوریک غلیظ در حضور اکسیژن حل میشود. لازم به ذکر است که مس در سری واکنشپذیری فلزات، پایینتر از منیزیم و روی قرار دارد، اما از نقره واکنشپذیرتر است و میتواند آن را از محلول نیترات نقره جابجا کند. در تماس با فلزات دیگر در حضور یک الکترولیت، مس میتواند دچار خوردگی گالوانیک شود.
حالت های اکسیداسیون رایج
مس معمولاً در ترکیبات خود دارای حالتهای اکسیداسیون +۱ (Cu⁺ یا cuprous) و +۲ (Cu²⁺ یا cupric) است که حالت +۲ پایدارتر و رایجتر میباشد. در شرایط خاص، حالت اکسیداسیون +۳ نیز ممکن است مشاهده شود. یون Cu²⁺ که رایجترین یون مس است، معمولاً در محلولهای آبی رنگ آبی ایجاد میکند، در حالی که ترکیبات مس(I) به طور کلی بیرنگ هستند.
واکنش ها با عناصر و ترکیبات دیگر
مس با اکسیژن واکنش داده و اکسیدهای مس مانند اکسید مس(I) (Cu₂O) و اکسید مس(II) (CuO) را تشکیل میدهد. همچنین با کلرید هیدروژن واکنش داده و کلرید مس(I) (CuCl) و آب تولید میکند. واکنش مس با اسید نیتریک منجر به تولید نیترات مس، دی اکسید نیتروژن و آب میشود.
در واکنش با گوگرد، سولفید مس(I) (Cu₂S) تشکیل میگردد. مس با یونهای هیدروکسید واکنش داده و هیدروکسید مس(II) (Cu(OH)₂) را به صورت رسوب تولید میکند. این فلز همچنین با آمونیاک واکنش داده و کمپلکسهای آمین مس را تشکیل میدهد و با یونهای کربنات، کربنات مس(II) (CuCO₃) را به صورت رسوب به وجود میآورد.

دلیل ارزشمند بودن فلز مس در صنایع امروزی
ارزش فلز مس در صنایع امروزی به دلیل ترکیبی از ویژگیهای منحصربهفرد آن است.
رسانایی الکتریکی بالا
مس بالاترین رسانایی الکتریکی را در بین فلزات غیر گرانبها دارد. این ویژگی به آن اجازه میدهد تا جریان الکتریکی را با کارایی بسیار بالا منتقل کند و در مقایسه با آلومینیوم، میتواند جریان بیشتری را در سطح مقطع کمتری حمل کند. به همین دلیل، مس به عنوان استاندارد بینالمللی برای مقایسه سایر رساناهای الکتریکی در نظر گرفته میشود. در دنیای امروز که به طور فزایندهای به الکتریسیته وابسته است، رسانایی الکتریکی برتر مس برای انتقال کارآمد انرژی و عملکرد بیشمار دستگاههای الکتریکی و الکترونیکی از اهمیت بالایی برخوردار است. کارایی آن در بسیاری از کاربردها از جایگزینهای ارزانتر و فراوانتر مانند آلومینیوم بیشتر است.
رسانایی حرارتی بالا
مس انتخاب اول برای کاربردهای مبدل حرارتی است. این فلز قابلیت انتقال سریع گرما را دارد و به همین دلیل در سیستمهای تهویه مطبوع، رادیاتورهای خودرو و خنککنندههای پردازنده در کامپیوترها به طور گسترده استفاده میشود. رسانایی حرارتی عالی مس برای اتلاف و انتقال کارآمد گرما در کاربردهای صنعتی و مصرفی مختلف ضروری است و به عملکرد و طول عمر تجهیزات گوناگون، از موتورها گرفته تا قطعات الکترونیکی، کمک میکند.
مقاومت در برابر خوردگی
مس در برابر عوامل جوی و محیطی مانند رطوبت و اکسیداسیون مقاومت خوبی دارد. این فلز یک لایه اکسید محافظ بر روی سطح خود تشکیل میدهد که از خوردگی بیشتر جلوگیری میکند و طول عمر بالای محصولات مسی را تضمین میکند. مقاومت ذاتی مس در برابر خوردگی، قابلیت اطمینان و دوام طولانیمدت قطعات و سیستمهای مبتنی بر مس را در صنایع مختلف تضمین میکند و هزینههای نگهداری را کاهش داده و عمر مفید آنها را افزایش میدهد.
چکش خواری و مفتول پذیری
مس به راحتی قابلیت شکلدهی به سیمها و قطعات پیچیده را دارد. این ویژگی برای ساخت سیمهای برق و لولههای مسی ضروری است و امکان ایجاد طرحهای پیچیده در صنایع مختلف را فراهم میکند
قابلیت بازیافت
مس به طور کامل قابل بازیافت است و کیفیت خود را در فرآیند بازیافت از دست نمیدهد. تخمین زده میشود که حدود ۸۰ درصد از کل مس استخراج شده تاکنون هنوز در حال استفاده است و حدود یک سوم تقاضای جهانی از طریق بازیافت تامین میشود. در عصری که آگاهی از مسائل زیستمحیطی رو به افزایش است، قابلیت بازیافت بالای مس آن را به مادهای پایدار و از نظر اقتصادی مقرون به صرفه تبدیل میکند و نیاز به استخراج معادن جدید را کاهش داده و منابع طبیعی را حفظ میکند.
کاربردهای مهم فلز مس
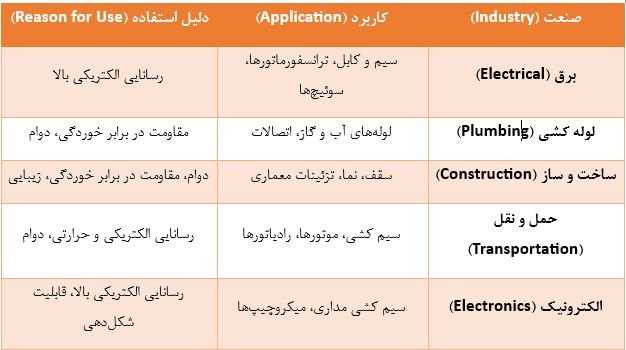
مس به دلیل خواص منحصربهفرد خود، در صنایع مختلف کاربردهای گستردهای دارد. بر اساس گزارشها، حدود ۶۵ درصد از مصرف جهانی مس در صنعت برق، ۲۵ درصد در ساخت و ساز، ۷ درصد در حمل و نقل و ۳ درصد در سایر صنایع به کار میرود.
سیم کشی برق
این کاربرد، مهمترین و گستردهترین مورد استفاده از مس است.۴ مس در ساخت انواع سیم و کابلهای برق، ترانسفورماتورها، سوئیچها، قطعات الکتریکی و اتصالات مداری مورد استفاده قرار میگیرد.۱ رسانایی الکتریکی بالای مس آن را به ایمنترین و کارآمدترین فلز برای انتقال جریان برق تبدیل کرده است.۱۴
لوله کشی
مس به طور گسترده در سیستمهای لولهکشی برای انتقال آب سرد و گرم، گازها و سایر مایعات استفاده میشود. مقاومت بالای مس در برابر خوردگی و دوام آن، این فلز را به گزینهای ایدهآل برای لولهکشی در ساختمانهای مسکونی و تجاری تبدیل کرده است.

ساخت و ساز
مس در بخش ساخت و ساز کاربردهای متنوعی دارد، از جمله استفاده در سقفها، نمای ساختمان (داخلی و خارجی)، چارچوب در و پنجره، ناودانها و به عنوان عناصر تزئینی معماری. دوام، مقاومت در برابر خوردگی و ظاهر زیبای مس، آن را به مادهای ارزشمند در این صنعت تبدیل کرده است. علاوه بر این، قابلیت بازیافت مس، آن را به یک انتخاب پایدار برای پروژههای ساختمانی تبدیل کرده است.
حمل و نقل
مس در صنایع حمل و نقل نیز کاربردهای فراوانی دارد. از آن در ساخت سیم کشی، موتورها، رادیاتورها، ترمزها، بلبرینگها و اتصالات در خودروها استفاده میشود. در هواپیماها نیز از مس در سیستمهای تهویه، هیدرولیک، ناوبری و سیم کشی استفاده میشود. با افزایش تولید خودروهای الکتریکی، تقاضا برای مس در این صنعت به طور چشمگیری افزایش یافته است، زیرا در این خودروها حدود چهار برابر بیشتر از خودروهای معمولی از مس استفاده میشود.
الکترونیک
مس به دلیل رسانایی الکتریکی عالی خود، جزء جداییناپذیر بسیاری از دستگاههای الکترونیکی است. این فلز در ساخت سیم کشی و اتصالات مداری، بردهای مدار چاپی، میکروچیپها، نیمهرساناها، مگنترونهای اجاقهای مایکروویو و الکترومغناطیسها کاربرد دارد. در مدارهای مجتمع، مس به دلیل رسانایی بهتر نسبت به آلومینیوم، به طور فزایندهای جایگزین آن در تراشههای سیلیکونی برای اتصالات شده است.
چالش های کار با فلز مس چیست؟
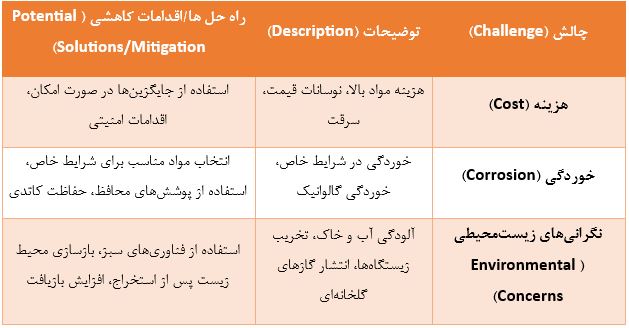
با وجود مزایای فراوان، کار با فلز مس چالشهایی نیز به همراه دارد.
هزینه
هزینه مواد اولیه مس در مقایسه با برخی فلزات دیگر مانند آلومینیوم بالاتر است. همچنین، قیمت مس در بازار جهانی نوسانات زیادی دارد که میتواند بر برنامهریزی و هزینههای پروژهها تاثیر بگذارد. ارزش بالای ضایعات مس متاسفانه میتواند منجر به سرقت و خرابکاری تاسیسات مسی شود. بررسیها نشان میدهد که تا زمانی که قیمت مس از حدود ۱۹ هزار دلار در هر تن تجاوز نکند، همچنان مقرون به صرفهترین فلز برای انتقال انرژی باقی میماند، اما با افزایش قیمت، آلومینیوم ممکن است از نظر اقتصادی جذابتر شود.
خوردگی در شرایط خاص
اگرچه مس به طور کلی در برابر خوردگی مقاوم است، اما در شرایط محیطی خاص میتواند دچار خوردگی شود. قرار گرفتن در معرض هوا و رطوبت میتواند منجر به تشکیل لایهای سبزرنگ به نام پتینه (کربنات مس) شود که اگرچه از نظر برخی افراد زیباست، اما ممکن است از نظر زیباییشناختی برای همه مطلوب نباشد و در طول زمان میتواند منجر به بیثباتی ساختاری شود. در تماس با فلزات غیر مشابه در حضور یک الکترولیت، مس مستعد خوردگی گالوانیک است. انواع دیگری از خوردگی مانند خوردگی حفرهای و بین دانهای نیز ممکن است در مس رخ دهد.
محیطهای با رطوبت بالا، تغییرات دما و وجود آلایندهها میتوانند سرعت خوردگی مس را افزایش دهند. کیفیت آب، به ویژه میزان اسیدیته، قلیائیت و غلظت کلرید آن، نقش مهمی در خوردگی لولههای مسی ایفا میکند. همچنین، خوردگی ناشی از میکروارگانیسمها (MIC) میتواند در لولههای مسی رخ دهد. خاکهای با غلظت بالای سولفات یا کلرید نیز میتوانند برای مس خورنده باشند. علاوه بر این، جریانهای سرگردان DC در زمین و آلودگی هوا ناشی از ترکیباتی مانند H₂S نیز میتوانند بر خواص سطحی مس و فرآیند لحیم کاری آن تاثیر منفی بگذارند.
نگرانی های زیست محیطی
استخراج و استفاده از مس نگرانیهای زیستمحیطی قابل توجهی را به همراه دارد. فرآیند استخراج معادن مس میتواند منجر به آلودگی منابع آبی با فلزات سنگین و مواد شیمیایی شود. معدنکاری روباز میتواند باعث تخریب خاک و از بین رفتن پوشش گیاهی در مناطق وسیعی شود. فرآیند ذوب مس و سایر مراحل تولید آن، مقادیر زیادی گازهای گلخانهای مانند دیاکسید کربن و دیاکسید گوگرد را وارد اتمسفر میکند.
استخراج مس در برخی مناطق میتواند اثرات منفی بر اکوسیستمهای طبیعی داشته و منجر به کاهش تنوع زیستی شود.مدیریت پسماندهای حاصل از معادن مس نیز یکی از چالشهای مهم زیستمحیطی است. قرار گرفتن در معرض مواد شیمیایی سمی در معادن مس میتواند خطراتی برای سلامت انسان به همراه داشته باشد. برای کاهش این اثرات منفی، نیاز به قوانین و مقررات مناسب و همچنین توسعه فرآیندهای تولید پایدار و افزایش بازیافت مس ضروری است. خوشبختانه، قابلیت بازیافت بالای مس به کاهش اثرات منفی آن بر محیط زیست کمک شایانی میکند.
نتیجه گیری
فلز مس با تاریخچهای غنی و خواص فیزیکی و شیمیایی منحصربهفرد خود، همچنان نقش حیاتی در صنایع مدرن ایفا میکند. رسانایی الکتریکی و حرارتی بالا، چکشخواری، مفتولپذیری و مقاومت در برابر خوردگی، این فلز را به مادهای بینظیر برای کاربردهای گسترده در زمینههای مختلف از سیم کشی برق و لوله کشی گرفته تا ساخت و ساز، حمل و نقل و الکترونیک تبدیل کرده است.
با این حال، چالشهایی نظیر هزینه، خوردگی در شرایط خاص و نگرانیهای زیستمحیطی مرتبط با استخراج و استفاده از مس نیز وجود دارند که نیازمند توجه و راهکارهای مناسب هستند. قابلیت بازیافت بالای مس، یک مزیت مهم در راستای پایداری و کاهش اثرات منفی زیستمحیطی آن به شمار میرود. با ادامه پیشرفت فناوری و افزایش تقاضا برای انرژی و زیرساختهای نوین، اهمیت فلز مس در آینده نیز همچنان پابرجا خواهد بود.

